Las baterías son productos muy difíciles de mejorar, por la base de su funcionamiento y por las condiciones en las que se quiere que operen. Una magnífica ilustración de esto lo tuvimos el pasado 29 de julio con la inauguración de la Gigagfábrica Tesla, una gigantesca fábrica de baterías en Nevada (Estados Unidos). Según su propietario, Elon Musk, Tesla había construido esa fábrica gigantesca porque era muchísimo más difícil obtener más rendimiento de las baterías que optimizar el proceso por el que se fabrican.
Irónicamente, la misma semana aparecía un artículo en Nature Energy en el que se describían los principios según los cuales se podría construir una batería cuyo prototipo almacena hasta el doble (y podría llegar a más) de la energía que las mejores baterías de ion-litio que fabricará la Gigafábrica. La nueva batería, desarrollada por un equipo de investigadores encabezado por Zhi Zhu, del Massachusetts Institute of Technology (Estados Unidos), todavía no es comercializable, pero su diseño es de esos que a priori no deberían dar problemas para llevarlos a escala industrial.
La batería litio-aire es el santo grial de la investigación en almacenamiento de energía desde los años setenta
La idea fundamental tras la nueva batería no es precisamente nueva. Es una versión de lo que se conoce como batería litio-aire, algo así como el santo grial de la investigación en almacenamiento de energía desde los años setenta. En pura teoría, estas baterías podrían contener más de cuatro veces la energía por kilogramo que contienen las baterías de ion-litio. El problema siempre ha sido fabricarlas. Como sugiere su nombre, dependen del aire o, más exactamente, del oxígeno del aire; otros componentes de éste, el vapor de agua o el dióxido de carbono, terminan dañándolas.
Incluso las versiones que funcionan con oxígeno puro también terminan teniendo problemas. Uno no pequeño es que el uso y recarga de las baterías de litio-aire existentes emplea una cantidad enorme de energía, ya que la recarga implica transformar el oxígeno gaseoso en lo que es, básicamente, un sólido, para volver a iniciar el ciclo. Aproximadamente el 30% de la energía empleada se pierde en este proceso. Además, los cambios en volumen que están asociados al cambio de gas a sólido y a gas otra vez, terminan debilitando los electrodos de la batería hasta el punto de que degeneran rápidamente, inutilizándola.
¿Qué tiene entonces de diferente la batería de Zhu et al? Pues que no usa aire real. El oxígeno se almacena dentro de la batería herméticamente cerrada en forma de un compuesto químico llamado superóxido de litio (LiO2; el óxido de litio convencional es Li2O).
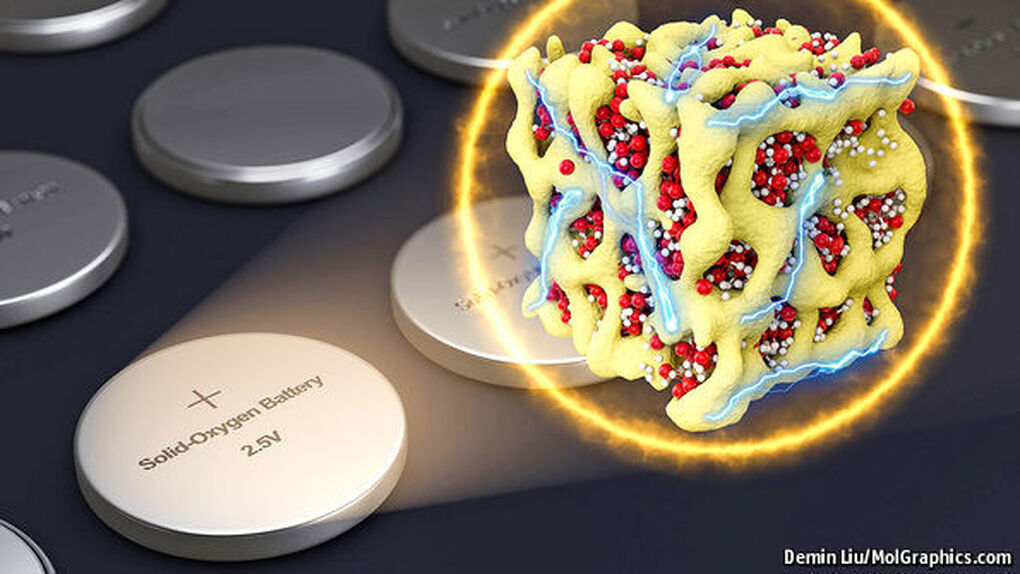
El superóxido es muy inestable, por lo que libera el oxígeno con facilidad. Para evitar que el superóxido se descomponga totalmente de forma espontánea, está distribuido en los huecos de una matriz hecha de óxido de cobalto (en la imagen representada por la estructura amarilla; las esferas blancas son los átomos de litio y las rojas los de oxígeno; con los trazos azules se supone que el artista quiere representar la electricidad), lo que aporta estabilidad al superóxido.
Cuando la nueva batería se está descargando, los iones de litio de un electrolito líquido que baña la matriz entran en el sólido y reaccionan con el oxígeno del superóxido para formar dos posibles compuestos, peróxido de litio (Li2O2) u óxido de litio (Li2O), ambos sólidos. Estas reacciones químicas impulsan los electrones a través de un circuito externo, donde pueden usarse para hacer funcionar cualquier cosa, desde un móvil a un coche.
Si la batería se conecta a la red, los electrones recorren el circuito en la otra dirección, las reacciones se invierten, regenerando el superóxido y tenemos la batería cargada de nuevo.
Los investigadores estiman que en un año podría existir un prototipo fabricable
Lo más impresionante de este nuevo diseño y su elemento más revolucionario es que el oxígeno siempre está en estado sólido, evitando de esta manera las transiciones sólido-gas-sólido que terminaban inutilizando las baterías anteriores, prolongando su vida útil de forma sustancial. En las pruebas con el prototipo se cargó y descargó 130 veces con solo un 2% de pérdida de capacidad. Además, en vez de un 30% de pérdida de energía estamos hablando de un 8%.
Desde un punto de vista ingenieril, llevar esta batería a producción comercial tiene las mismas dificultades que las baterías ion-litio, por lo que los investigadores estiman que en un año podría existir un prototipo fabricable. Parece realista: han empezado a hablar ya con fabricantes. Una batería más ligera, con mayor capacidad, significa coches y móviles más ligeros con más autonomía. Seguro que si cuaja nos enteraremos en un par de años vía publicidad.
Referencia: Zhi Zhu et al (2016) Anion-redox nanolithia cathodes for Li-ion batteries. Nature Energy doi: 10.1038/nenergy.2016.111
* Este artículo es parte de ‘Proxima’, una colaboración semanal de la Cátedra de Cultura Científica de la UPV con Next. Para saber más, no dejes de visitar el Cuaderno de Cultura Científica.


Ya no se pueden votar ni publicar comentarios en este artículo.