“No me voy a rendir y si hay algún tratamiento que se adapte a mí, quiero que experimenten conmigo”. Con estas duras palabras se manifestaba la malagueña Carolina Cerezo en distintos medios en busca de alguna vía para tratar el cáncer que le habían diagnosticado con 24 años. En redes sociales y en una carta dirigida a El País, la joven expresaba una desesperación por la que pasan cada año cientos de pacientes y sus familiares cuando se les diagnostica una enfermedad grave para la que los tratamientos aún no son efectivos. El caso de Carolina, que falleció a finales de mayo, se convirtió en un símbolo y un ejemplo más de la necesidad de informar a los pacientes de las vías que tienen a su disposición para acceder a estos tratamientos.
“Lo primero que hay que saber es que, efectivamente, un ensayo clínico es una posibilidad de optar a un tratamiento y que te puede llegar en un momento en que todavía puedas tener una oportunidad, pero también implica incertidumbre, ya que el efecto del tratamiento puede ser neutro o incluso negativo”, explica César Hernández García, jefe del Departamento de Medicamentos de Uso Humano de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). “Por otro lado, desgraciadamente, pedir que experimenten con uno no es tan fácil; o bien existe una línea de investigación sobre esa enfermedad a la que incorporarse o no se abre una línea para probar con un solo paciente”.
La decisión de participar en un ensayo clínico conviene hacerla apoyada por un médico
Eso no quiere decir que no haya otras alternativas, como el solicitar el tratamiento de uso compasivo si existe algo que se ha mostrado útil contra la enfermedad pero aún no ha sido aprobado. En cualquier caso, la decisión de participar en un ensayo clínico, insiste Hernández, conviene hacerla apoyada por un médico, que suelen estar al día de cuáles son las últimas investigaciones en marcha y disponen de los recursos necesarios. En caso de no estar de acuerdo con el diagnóstico y tratamiento, en España está garantizado el derecho a una segunda opinión médica por otro especialista y en otro centro, si así se requiere.
Para conocer si existen ensayos clínicos en marcha sobre la enfermedad que padecemos, existen varios recursos oficiales. El más útil y actualizado es el de la propia AEMPS, el Registro Español de Estudios Clínicos. Desde 2013 se han incorporado a este registro 5.056 ensayos realizados en centros españoles. Basta con introducir el nombre de la enfermedad para encontrar toda la información. Si uno busca “cáncer de mama”, por ejemplo, encontrará varios ensayos que están en fase de reclutamiento y otros que aún no se han iniciado, y en cada uno de ellos los criterios de inclusión y exclusión, así como los datos de contacto del promotor, que no siempre está en España. Entre los resultados encontramos un ensayo sobre el “cáncer de mama en etapa avanzada” que probará en 540 sujetos la eficacia de un fármaco contra un tipo concreto de este cáncer (HER2 positivo) y lo comparará con otros tratamientos. Todos los datos se pueden descargar en PDF y están escritos con un esfuerzo por hacerlos inteligibles.
El Registro Español de Estudios Clínicos permite buscar de manera sencilla qué ensayos están en marcha y en qué centros
“El registro está pensado para que sea accesible para todo el mundo”, explica Hernández. “Nosotros incluimos una cosa que no tienen otros registros, un resumen de 100 palabras en un lenguaje lego sobre cuál es el objetivo del ensayo clínico”. Este registro se puso en marcha tras el Real Decreto Legislativo 1/2015, en el que se hizo un gran esfuerzo para facilitar los procedimientos para aprobar ensayos clínicos y que ha supuesto un gran paso adelante. “Se trata de que los pacientes puedan acceder y preguntar a sus médicos, algo que ya ocurre de manera natural, no podemos poner puertas al campo”, explica el responsable de AEMPS.

El segundo nivel de consulta sobre ensayos clínicos disponibles es a una escala más amplia. Se trata del Registro de Ensayos Clínicos de la Unión Europea (EU clinical trials register), que depende de la Agencia Europea de Medicamentos (EMA). La desventaja es que está en inglés y la información parece de forma mucho menos clara, pero permite localizar todos los ensayos clínicos que se hayan realizado o se estén realizando en los países de la Unión Europea.
A un nivel global se encuentra el registro de los Institutos Nacionales de Salud de Estados Unidos (NIH). En Clinicaltrials.gov se pueden encontrar los ensayos clínicos que se están realizando en más de 190 países. Durante mucho tiempo, para cualquier investigador era requisito indispensable incluir su estudio en este registro si quería publicar los resultados en una revista científica, de modo que se ha convertido en la mayor base de datos del mundo de este tipo de estudios. Aquí también podemos ver el objetivo del ensayo, los datos de contacto de los coordinadores y participantes y su estado actual. Aunque no es habitual, en casos de enfermedades muy poco frecuentes las empresas están dispuestas a pagar el traslado y los gastos del paciente en el país donde se realiza el ensayo.
Las farmacéuticas también ponen las bases de datos con sus ensayos a disposición de los pacientes
Otra pata importante del sistema de información pública es la que aportan las propias compañías farmacéuticas, que ponen las bases de datos con los ensayos que están realizando a disposición de los pacientes. Es el caso de la compañía Lilly, que a través de la web Lillytrialguide y de la aplicación Trials4Me nos permite incluir el código postal junto con la enfermedad sobre la que estamos buscando ensayos y obtener una ubicación de los centros en un mapa de Google. Si uno busca información sobre tratamientos para el cáncer de páncreas metastásico, por ejemplo, puede llegar hasta un ensayo en marcha y leer los requisitos que se piden como paciente, los objetivos del trabajo y un botón para contactar directamente con cada centro.
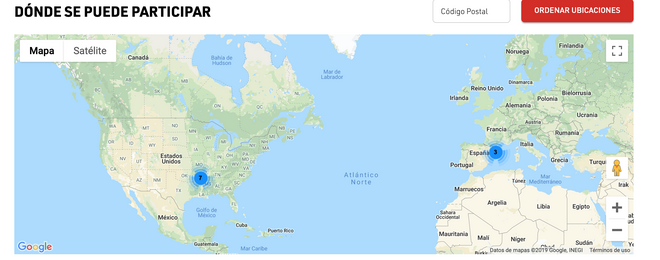
“La web está enfocada a los pacientes, de forma que tú pones la enfermedad que tienes y pones dónde vives y te sale el mapa de Google con todos los centros marcados de qué hospitales están investigando y la distancia”, explica José Antonio Sacristán, director médico de Lilly España. Él y su equipo llevan años haciendo un esfuerzo por llegar a las asociaciones de pacientes y poner a su disposición este conocimiento y estas herramientas, para desmitificar muchos aspectos sobre los ensayos clínicos. “Existen muchos prejuicios; que la investigación es peligrosa, que son conejillos de indias… Hay que desmitificarlo un poco”, explica. “Y sobre todo tener claro que los pacientes se pueden beneficiar ahora de tratamientos gracias a que otros pacientes del pasado participaron en ensayos clínicos. Es un poco por altruismo, y dicen los expertos en bioética que esa debe ser la principal motivación para participar”.
Registros de pacientes
Otra posible vía para participar en un ensayo clínico es la que acaba de iniciar la Junta de Andalucía con el Registro Voluntario de Personas Interesadas en Participar en Ensayos Clínicos en Andalucía (ReVECA) que permite crear una especie de “bolsa” de pacientes para los ensayos que vayan aprobándose. Se trata, según la propia Junta, de “una base de datos de gran utilidad para los equipos de investigación que necesiten a personas voluntarias” y un medio para que los pacientes puedan manifestar su voluntad de participar y les puedan contactar en caso de que haya un ensayo sobre su enfermedad.
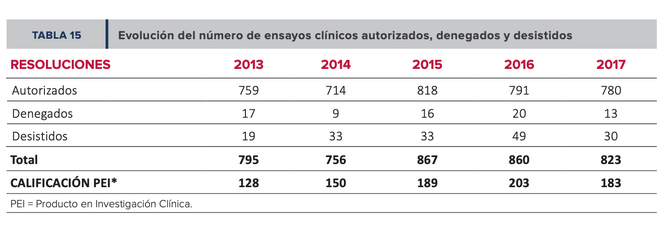
Durante el año 2017 se autorizaron 780 ensayos, se denegaron 13 y hubo 30 desistimientos
España cuenta además con organismos intermedios como la Plataforma Española de Unidades de Investigación Clínica y Ensayos Clínicos (SCReN) cuyo objetivo es “ayudar a los investigadores del sistema nacional de salud a llevar adelante ensayos”, según explica su coordinador, Emilio Vargas Castrillón. “Sabemos que hay una serie de cosas que a los investigadores les resultan difíciles, como la interacción con la AEMPS, los comités éticos, la documentación o los plazos, y les echamos una mano e intentamos que sea lo más sencillo para ellos”. Por todo esto, nuestro país está entre los que más ensayos clínicos tienen en marcha en Europa. Durante el año 2017 se autorizaron 780 ensayos, se denegaron 13 y hubo 30 desistimientos, según los últimos datos oficiales disponibles.
“Solo el 5% de los pacientes cuyo médico es a la vez investigador tiene acceso a los ensayos”
“España es un país atractivo porque tiene un sistema de salud muy potente, sus profesionales son muy buenos y ofrece la posibilidad de reclutar pacientes muy rápido”, indica César Hernández desde la AEMPS. “Sí que es verdad que han mejorado los trámites y con la nueva legislación los procesos son más ágiles”, confirma Sacristán desde el sector privado. “España ha hecho un esfuerzo, y también los hospitales, que se han dado cuenta del gran beneficio que supone para el sistema sanitario participar en ensayos clínicos”. ¿Significa esto que nuestro médico estará al día de qué tratamientos se están probando para nuestra enfermedad?
“El gran problema es que solo el 5% de los pacientes cuyo médico es a la vez investigador tiene acceso a los ensayos”, señala el director médico de Lilly. “Si tienes la suerte de que tu médico es investigador puedes participar. Con el otro 95% hay que buscar formas de que tengan información de que existen estas opciones. Pero cada vez existen más grupos de investigación dentro de las sociedades científicas, agrupaciones de pacientes… En general es más fácil acceder a la información”. En Estados Unidos, donde solo el 3% de los pacientes participan en ensayos clínicos sobre cáncer, el debate está también en la forma en que las personas acceden a la información y el papel de las redes sociales en esta búsqueda, ya que no siempre circulan datos fiables.
Tratamientos de uso compasivo
Otra posibilidad de los pacientes es recibir un tratamiento de uso compasivo, siempre que se trate de personas “que padecen una enfermedad crónica o gravemente debilitante o que se considera pone en peligro su vida y que no pueden ser tratados satisfactoriamente con un medicamento autorizado”. También se puede autorizar el tratamiento con un medicamento que se está probando con éxito en un ensayo clínico pero en el que el paciente no ha podido participar.
Ante una enfermedad grave, el médico puede pedir que se autorice a su paciente a tomar un fármaco
En todo caso, el propio fabricante del medicamento debe autorizar su uso compasivo y el médico tiene que hacer la solicitud a través del formulario correspondiente para que la AEMPS lo apruebe, tal y como se establece en el RD 1015/2009 sobre disponibilidad de medicamentos en situaciones especiales. Además, el facultativo está obligado a justificar el motivo por el que ese paciente no puede tratarse de forma satisfactoria con las alternativas terapéuticas autorizadas, aportar los datos que apoyan el uso del medicamento para el paciente y las razones por las cuales el paciente no puede ser incluido en un ensayo clínico.
“Son medicamentos que están en investigación y aún no han sido autorizados, pero existen indicios de que pueden tener una eficacia”, indica Sacristán. “También se le aplica a pacientes que han participado en un ensayo clínico que ha tenido buen resultado. Cuando termina, pasa un tiempo hasta que se aprueba el medicamento, y ahí el uso compasivo consiste en continuar el tratamiento de esos pacientes hasta que el tratamiento se apruebe”. A menudo, es la propia compañía la que suministra ese fármaco sin coste alguno.
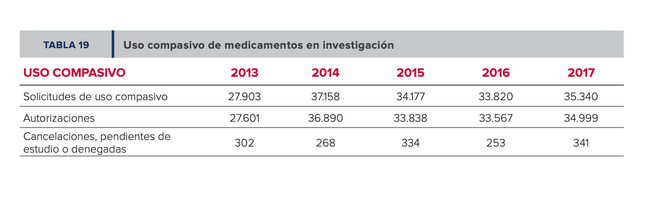
Como se recoge en la memoria anual de la agencia, cada año se reciben entre 30.000 y 35.000 solicitudes para pacientes y la inmensa mayoría son aprobadas. En la práctica clínica, hay decenas de ejemplos de medicamentos que se usan así, sobre todo en oncología, como el Everólimus para cáncer de riñón metastásico, el acetato de abiratenona para el cáncer de próstata o el Ipilimumab para el melanoma metastásico. Asimismo, como señala la profesora de farmacología de la Universidad de Málaga Encarnación Blanco-Reina en una revisión sobre el tema, “la práctica de prescribir medicamentos fuera de las condiciones de uso autorizadas puede entrañar beneficios, pero también riesgos, a veces muy importantes para el paciente”, y en una parte de los casos la eficacia terapéutica no tiene suficiente respaldo científico, de modo que conviene ser cautelosos.


Ya no se pueden votar ni publicar comentarios en este artículo.