Todos y cada uno de nosotros tiene un cuerpo único y diferenciado del resto de humanos de nuestra especie, y no solo en aspecto físico sino también a nivel genómico. Ello es debido a que todas las células que lo conforman son, a su vez, únicas, derivadas de una célula inicial (el zigoto) procedente de la fusión de óvulo y espermatozoide, y cuyo genoma se construye con los 23 cromosomas de nuestro padre y los 23 de nuestra madre. Dado que todas las células de nuestro cuerpo derivan de este zigoto mediante un gran número de divisiones celulares, cabría esperar que todas ellas poseyeran el mismo genoma.
Sin embargo, si observamos con detalle grupos de células de cualquiera de nuestros tejidos puede que no apreciemos un conjunto uniforme sino más bien un «patchwork», un mosaico celular. Esto se debe a que se producen mutaciones en los genomas de algunas células a medida que acumulamos divisiones celulares. Si las células que sufren estas mutaciones siguen dividiéndose, forman agrupaciones con un genoma diferenciado (denominadas clones somáticos) dentro de un tejido concreto. En algunos casos, estos clones pueden acumular mutaciones perjudiciales y convertirse en tumores. Esta idea se confirma con un estudio que acaba de publicar Science y que nos acerca al objetivo de detectar tumores antes de que se formen.
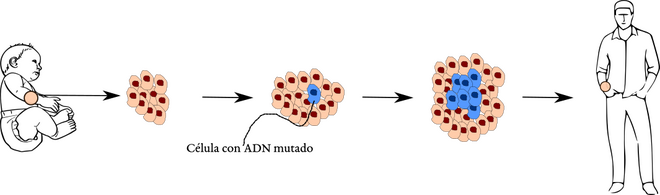
Para este estudio, un grupo de investigadores del Broad Institute en el MIT y Harvard (EE.UU.) utilizaron la base de datos del portal GTEx, en el que se encuentran datos de secuenciación de ARN y ADN de distintos tejidos humanos de más de 600 personas fallecidas por causas distintas al cáncer. El ARN es la secuencia que copia la información de cada gen concreto requerido para el funcionamiento de una célula y supone el paso intermedio para su traducción a una proteína funcional.
Se encontraron clones con mutaciones en prácticamente todos los donantes del estudio (467 de 488)
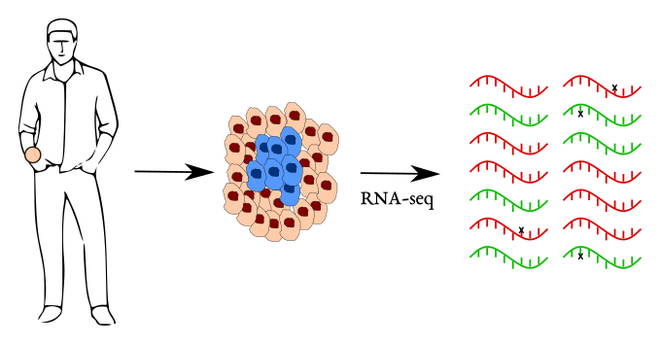
Utilizando datos de 488 personas que abarcaban 29 tipos de tejidos, estos investigadores calcularon para cada muestra de tejido de cada donante qué fracción del ARN expresado presentaba alguna mutación (la denominada fracción alélica). Pongamos un ejemplo: imaginemos que contamos las secuencias de ARN que expresan dos genes distintos (en la siguiente figura, en rojo y verde). Si contamos cuántas secuencias tienen alguna mutación que las diferencie de la mayoría (las que están marcadas con una cruz) nos encontramos con que la fracción alélica del gen rojo es 2/8=0,25 y la del gen verde 2/6=0,33. Pensemos que para la secuenciación de ARN se utilizan muestras macroscópicas de tejidos, que pueden llegar a incluir cientos de miles de células.
Mediante este análisis se encontraron clones con mutaciones en prácticamente todos los donantes del estudio (467 de un total de 488 personas), así que podemos suponer que la mayoría de nosotros presenta estos clones celulares. Los clones se detectaron en todos los tejidos analizados, aunque aquellos que acumulaban más mutaciones eran piel, pulmones y mucosa esofágica. Los autores sugieren que una exposición a factores ambientales (radiación ultravioleta, polución, tabaco…) puede ser la causa de la mayor carga mutagénica de estos tejidos.
Además, algunas de las mutaciones detectadas en estos clones se encontraban en genes asociados a determinados tipos de cáncer, por lo que podrían posteriormente inducir un crecimiento celular descontrolado que formaría un tumor. En concreto, se observaron un mayor número de mutaciones en los genes TP53 y NOTCH1, que fabrican proteínas que actúan como supresores de tumores, con una mayor incidencia en piel y esófago.
Se observó que el número de clones y de mutaciones aumentaba con la edad del donante
También se observó que el número de clones y de mutaciones aumentaba con la edad del donante, sobre todo en esófago y piel. Este resultado era de esperar, ya que a mayor edad se han acumulado un mayor número de divisiones celulares y se ha sufrido una mayor exposición ambiental. En el caso de la piel, el número de clones era mayor en tejidos más expuestos al sol. Este aumento con la edad de clones en tejidos podría tener alguna contribución a enfermedades asociadas al envejecimiento.
La identificación de clones somáticos no es nueva. Estudios anteriores ya encontraron agrupamientos de células mutadas en piel y esófago. La novedad de este artículo radica en la utilización de una mayor cantidad de muestras ya secuenciadas y existentes en bases de datos públicas, y que refuerza el conocimiento existente para la prevención del desarrollo de tumores.
Pese a la relevancia del estudio, cabe hacer un par de matizaciones. En primer lugar, el análisis de mutaciones se hace utilizando un procedimiento bioinformático que, tal y como los autores indican, presenta un gran número de falsos positivos (muchas de las mutaciones que se detectan no existen realmente), aunque sí sirva para detectar un mayor número cualitativo de mutaciones en algunos tejidos. Para confirmar si estas mutaciones son reales habría que utilizar otro tipo de técnicas genéticas para validarlas experimentalmente, es decir, habría que mirar una a una si las mutaciones están en la posición que indica el programa informático. Aún así, esto no resta validez a los resultados.
Ahora hay que estudiar en qué condiciones específicas estos clones pueden convertirse en tumores
En segundo lugar, al analizar las variaciones en el ARN expresado no se localizan las mutaciones que pudiera haber en regiones del genoma que no codifican proteínas. Estas regiones son importantes ya que en ellas se encuentran elementos que ayudan a la expresión génica y mutaciones en estas localizaciones también podrían ser responsables de producir tumores. Del mismo modo, este método no es capaz de detectar mutaciones en genes con un bajo nivel de expresión o clones con un pequeño número relativo de células, ya que en ese caso un excesivo ruido en la medida no permitiría la identificación de mutaciones.
Así pues, este estudio confirma la hipótesis de que nuestros tejidos contienen clones celulares con ADN diferenciado que, al acumular más mutaciones, podrían dar origen a un tumor. Es necesario ahora dirigir las investigaciones a conocer en qué condiciones específicas estos clones pueden convertirse en tumores, es decir, distinguir cuáles de estos grupos de células corren riesgo de desarrollar un cáncer para así poder prevenirlo.
Referencia: RNA sequence analysis reveals macroscopic somatic clonal expansion across normal tissues, Keren Yizhak et al. Science 07 Jun 2019: Vol. 364, Issue 6444. DOI: 10.1126/science.aaw0726


Ya no se pueden votar ni publicar comentarios en este artículo.