Eric Betzig, ganador del premio Nobel de química en 2014, no es de esos investigadores que, una vez conseguido el Nobel, se dedican exclusivamente a dar conferencias por el mundo. Ahora, con un equipo de colaboradores del Instituto Médico Howard Hughes (EE.UU.), acaba de presentar una variante de la técnica de microscopía de superrresolución que le valió el premio, con la que consigue visualizar por primera vez procesos dinámicos dentro de la membrana de una célula, lo que es equivalente a decir que permite “ver” moléculas en movimiento. La investigación se publica en Science.
Consigue mitigar el daño que la exploración en la célula.
Betzig, junto con Stefan Hell y W.E. Moerner, recibieron conjuntamente el premio Nobel el año pasado por conseguir superar el límite de difracción de un microscopio de fluorescencia. Mientras que la técnica desarrollada por Hell eliminaba la fluorescencia en un área de un nanómetro de diámetro para obtener una imagen en superrresolución de una célula, Betzig y Moerner, trabajando por separado, investigaron la posibilidad de hacer aparecer y desaparecer la fluorescencia en moléculas individuales a voluntad.
Betzig y sus colegas lo que han hecho ahora es refinar esta técnica basada en el interruptor de la fluorescencia, conocida como SIM (de las siglas en inglés de microscopía de iluminación estructurada), para crear un nuevo método llamado SIM no lineal de fotoactivación pautada. Esto no significa otra cosa que, en vez de iluminar la muestra entera como hace la SIM, ahora lo que se hace es iluminar un pequeño subconjunto de moléculas de la muestra, obteniendo imágenes en una fracción del tiempo que se emplea usando la SIM estándar. A esto se añade una apertura ultra-alta con lo que la resolución de la SIM pasa de 100 nm a 84 nm. Además esta forma de proceder consigue mitigar el daño que la exploración supone para la célula.
Permite visualizar el movimiento de diferentes proteínas.
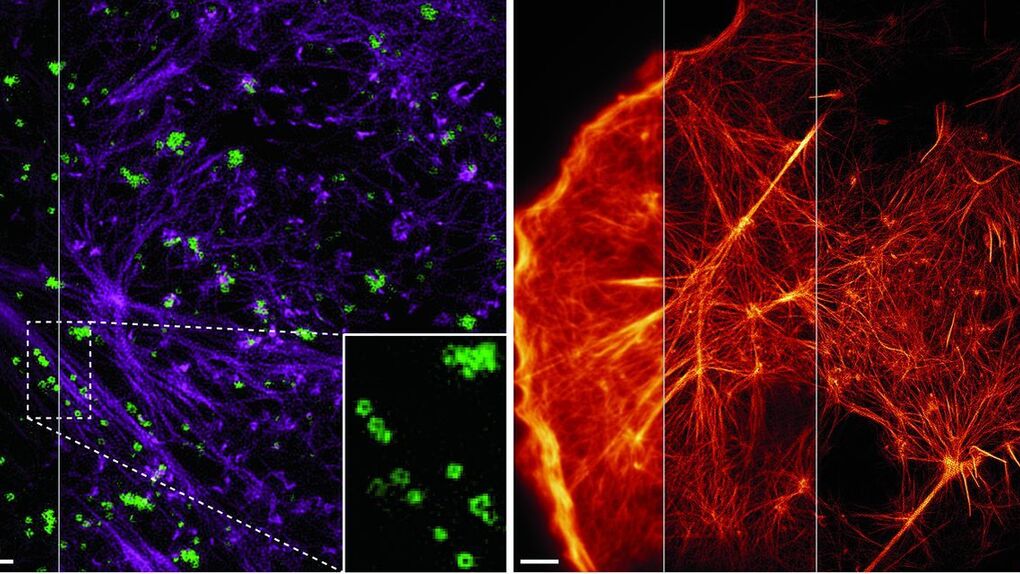
El uso de esta técnica de iluminación de alta velocidad permite a los investigadores visualizar el movimiento de diferentes proteínas, como la clatrina y la caveolina, simultáneamente y ver cómo interaccionan para facilitar el transporte a través de la membrana celular.
Esta técnica llega ya a extremos que hace solo unos años habrían sido clasificados de ciencia ficción, si no directamente fantasiosos por imposibles. Las consecuencias que puede tener su uso en investigación biológica y médica son espectaculares.
Referencia: Dong Li et al (2015) Extended-resolution structured illumination imaging of endocytic and cytoskeletal dynamics (Science) DOI: 10.1126/science.aab3500
* Este artículo es parte de ‘Proxima’, una colaboración semanal de la Cátedra de Cultura Científica de la UPV con Next. Para saber más, no dejes de visitar el Cuaderno de Cultura Científica.


Ya no se pueden votar ni publicar comentarios en este artículo.