A estas alturas de la película todos hemos oído hablar en alguna ocasión de que muy posiblemente el coche del futuro será uno que consumirá hidrógeno. Y esto tendría muchas ventajas frente al eléctrico: no son necesarias baterías que son muy pesadas y quitan espacio, la potencia sería mucho mayor, al igual que la autonomía y la contaminación sería nula. Pero no todo es tan bonito: el principal inconveniente para el desarrollo de esta tecnología es obtener el propio hidrógeno. Aunque es posible que esto cambie pronto.
El hidrógeno molecular es el combustible más limpio que existe
Si bien el hidrógeno es el elemento más abundante, con diferencia, del universo, es tan ligero que la gravedad de la Tierra no es suficiente para retenerlo y escapa al espacio. Y es una pena, porque el hidrógeno molecular (H2) es el combustible más limpio que existe: al quemarlo en el aire solo produce agua y energía, nada más. Pero como solo existen trazas de él en la atmósfera la mayor parte del hidrógeno que se emplea como combustible hoy día procede de los combustibles fósiles (petróleo y gas natural mayormente), con los que se emplean procesos como el reformado catalítico del petróleo.
Una opción mucho más ecológica y sostenible de obtener hidrógeno es extraerlo termoquímicamente de la biomasa, usando altas temperaturas y catalizadores, eso sí, muy caros. Aunque existen alternativas como la fermentación, la electrolisis y la conversión fotoelectroquímica, estos métodos no pueden con las moléculas que forman la mayor parte en peso de la biomasa, la lignina y la celulosa presentes en hierbas y maderas, con lo que la eficiencia se evapora.
Ahora, un equipo de investigadores encabezado por Wei Liu, del Instituto de Tecnología de Georgia (EE.UU.), han presentado una tecnología electrolítica que puede extraer hidrógeno a partir de casi cualquier tipo de biomasa.
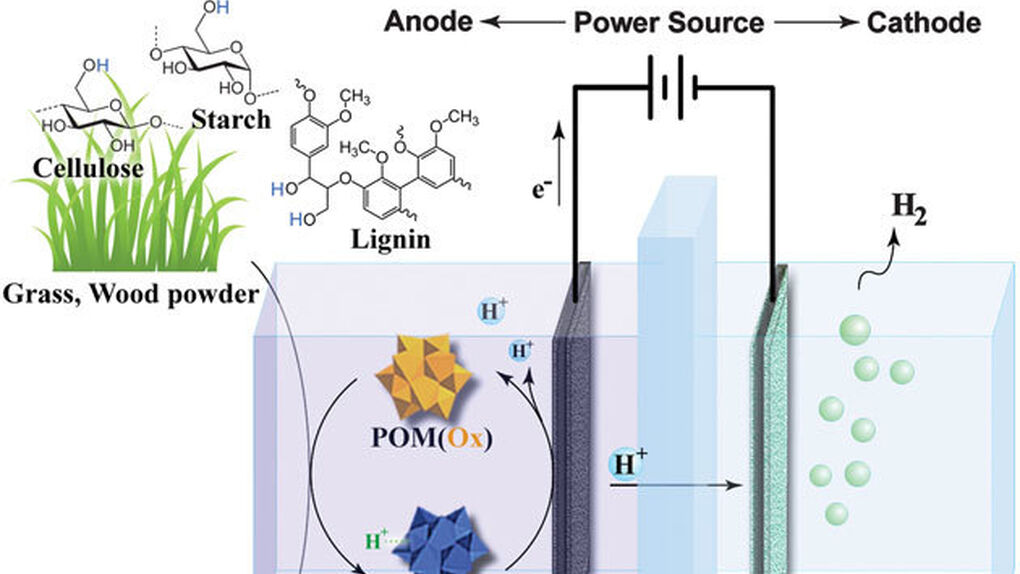
El proceso tiene lugar en una cuba eletrolítica que contiene una membrana, que los protones (iones de hidrógeno, H+) pueden atravesar, colocada entre dos placas que son el ánodo y el cátodo. Una dispersión en agua de biomasa en polvo y un catalizador (polioxometalato o POM) se añaden a la parte del ánodo de la cuba. Calentando esta mezcla o, simplemente exponiéndola al sol, las moléculas de POM se encargan de arrancar átomos de hidrógeno de la biomasa, convirtiéndose en H-POM.
No descartan mejorar el proceso para obtener eficiencias cercanas al 100%.
Si ahora se aplica un voltaje entre los electrodos, las moléculas H-POM dejan un electrón en el ánodo cargado positivamente y abandonan el protón a su suerte en el agua. Los electrones fluyen por el circuito hasta el cátodo de la cuba, a donde los protones solitarios han llegado atravesando la membrana, que se encarga de que nada más les acompañe. Protones y electrones se combinan en el cátodo, formando átomos de hidrógeno (H), que reaccionan entre sí rápidamente para formar hidrógeno molecular (H2) que ya puede ser recogido y almacenado.
Esta metodología abre la puerta a una producción de hidrógeno ajustable a la cantidad y variedad de biomasa disponible, con lo que ello implica para la posibilidad de producir localmente hidrógeno en pequeñas instalaciones donde exista biomasa disponible y se consuma también localmente. Los investigadores son muy optimistas y no descartan mejorar el proceso para obtener eficiencias cercanas al 100%. Ya están en marcha en la búsqueda de un colaborador industrial para construir una primera planta piloto.
Referencia: W. Liu et al (2016) High efficiency hydrogen evolution from native biomass electrolysis Energy Environ. Sci. DOI: 10.1039/C5EE03019F
* Este artículo es parte de ‘Proxima’, una colaboración semanal de la Cátedra de Cultura Científica de la UPV con Next. Para saber más, no dejes de visitar el Cuaderno de Cultura Científica.


Ya no se pueden votar ni publicar comentarios en este artículo.